Naprej: kalorimetrija Navzgor: toplota Nazaj: T raztezanje Kazalo
hmmm...bolje bi bilo:
iz plinske enačbe pV = m/MRT izrazimo prostornino :
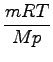 =
=  = 24, 3m3
= 24, 3m3
?pa saj menda ni tako težko?ali pač!
![\includegraphics[width=231pt]{plinska-1}](img247.gif)
|
![]() V =
V = ![]() V
V![]() T oziroma
T oziroma
![]() =
= ![]() V = konst.
V = konst.
Razmerje med spremembo prostornine in spremembo temperature lahko izrazimo tudi iz plinske enačbe:
![]() = konst. ali če je tlak konstanten:
= konst. ali če je tlak konstanten:
![]() = konst.
= konst.
s pomočjo grafa V(T) lahko vidimo, da mora biti
![]() =
= ![]()
lahko pa tudi izračunamo:
končna prostornina:
Vk = ![]() Tk
Tk
sprememba prostornine:
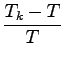
zato je razmerje
ko primerjamo enačbi:
oziroma
gostota= 0,17 kg/m3
vstavimo podatke:
T = 100oC = 373K
m = 2kg
M = 28kg/(kmol )
R = 8314J/(kmolK)
p1 = 2bara = 2105N/m2
p2 = 0, 5bara = 0, 5105N/m2
dobimo prostornini:
V1 = 1, 11m3
V2 = 4, 43m3
vstavimo podatke:
p = 1, 5bara = 1, 5105N/m2
m = 3kg
M = 32kg/(kmol )
R = 8314J/(kmolK)
T1 = 27oC = 300K
T2 = 327oC = 600K
dobimo prostornini:
V1 = 1, 56m3
V2 = 3, 12m3
Plinska enačba pV = NkT nam pove, da je tlak plina sorazmeren s temperaturo plina
p ![]() T, če je prostornina konstantna. Steklena bučka se skrči, ko se ohladi, vendar smemo to spremembo prostornine zanemariti. Ker se temperatura plina v žarnici zmanjša za 4× se m ora prav tolikokrat zmanjšati tudi tlak. Torej bo tlak v žarnici, ko se le-ta ohladi
p =
T, če je prostornina konstantna. Steklena bučka se skrči, ko se ohladi, vendar smemo to spremembo prostornine zanemariti. Ker se temperatura plina v žarnici zmanjša za 4× se m ora prav tolikokrat zmanjšati tudi tlak. Torej bo tlak v žarnici, ko se le-ta ohladi
p = ![]() Pa = 0, 75Pa.
Pa = 0, 75Pa.
Zgolj iz radovednosti izračunam še spremembo prostornine steklene žarnice (temperaturni razteznostni koeficient za steklo pri T = 20oC:
0, 85 . 10-5K-1,
![]() = 1 . 10-5K-1,
7, 6 . 10-6st-1; zanimivo, koliko različnih vrednosti).
Prva težava, ki jo srečam je vprašanje, koliko je temperaturni koeficient raztezka. Najdem samo vrednosti za 20oC, ne pa tudi za 1200K ali 300KC; in najbrž je temperaturni odvisen od temperature. Vzamem največjo vrednost, ki sem jo našel
= 1 . 10-5K-1,
7, 6 . 10-6st-1; zanimivo, koliko različnih vrednosti).
Prva težava, ki jo srečam je vprašanje, koliko je temperaturni koeficient raztezka. Najdem samo vrednosti za 20oC, ne pa tudi za 1200K ali 300KC; in najbrž je temperaturni odvisen od temperature. Vzamem največjo vrednost, ki sem jo našel
![]() = 1 . 10-5K-1 in izračunam:
= 1 . 10-5K-1 in izračunam:
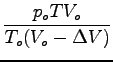 = 0, 77Pa
= 0, 77Pa
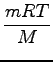
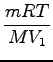 = 0, 305 . 105
= 0, 305 . 105Točki vnesemo v graf in ju povežemo z lepo hiperbolo (slika 29).
me 2007-11-05